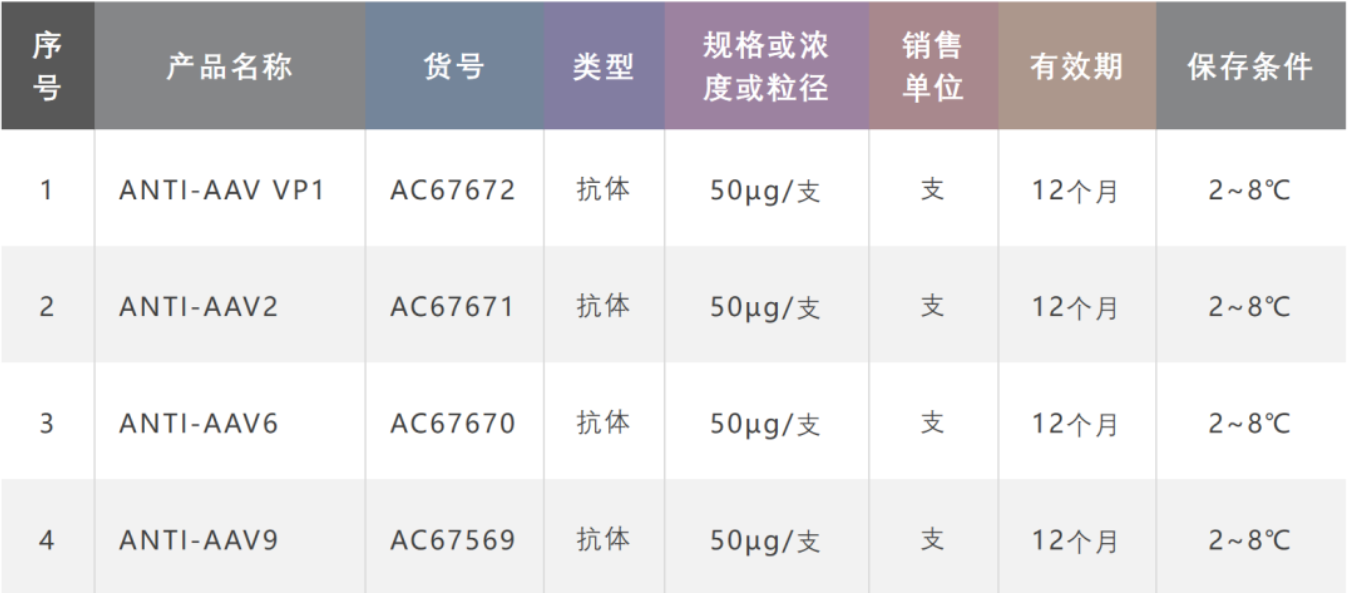
腺相关病毒(AAV)属于细小病毒科,是一种安全性高、免疫原性低、宿主范围广、表达稳定和性质稳定的非致病性ssDNA病毒属小型无包膜病毒,被广泛用作基因治疗的载体。Acnovia目前提供AAV2、6、9血清型的腺相关病毒(AAV)和AAV(VP1)抗体,可特异性识别完整的病毒衣壳以及AAV病毒亚基和复制品的特异性抗体,还将提供用于相关 AAV 亚型的滴定 ELISA 试剂盒。
AAV 基因组结构、DNA 复制和病毒组装
第一个人类腺相关病毒(AAV)于1965年被发现,是腺病毒(Ad)制剂的污染物。AAV 是最小的病毒之一,其非包膜二十面体衣壳约为 22 nm。尽管AAV在人群中的血清阳性率很高(大约80%的人类为AAV2血清阳性),但该病毒与任何人类疾病无关。AAV具有约4.7千碱基(kb)的线性单链DNA(ssDNA)基因组,在末端有两个145个核苷酸长的倒置末端重复序列(ITR)。该病毒不编码聚合酶,因此依赖于细胞聚合酶进行基因组复制。ITRs位于两个病毒基因的两侧 - rep(复制)和“cap(衣壳),分别编码非结构和结构蛋白(1)。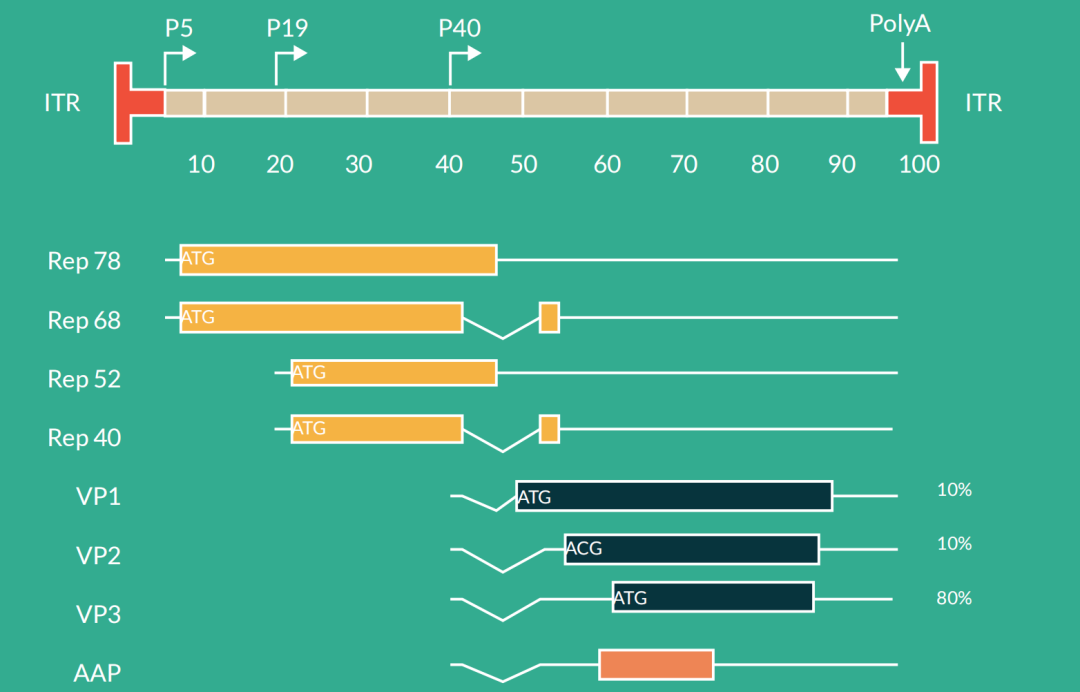
图1.AAV基因组和蛋白结构
Cap基因通过交替剪接和翻译起始产生三种衣壳蛋白VP1(病毒粒子蛋白1)、VP2和VP3,分子量分别为87、72和62 kDa,这些衣壳蛋白组装成60个亚基的近球形蛋白质壳。通过使用两个启动子和选择性剪接,rep基因编码四种调节蛋白,分别称为Rep78,Rep68,Rep52和Rep40,这些蛋白质参与AAV基因组复制。
腺相关病毒AAV载体的应用
从历史上看,大多数重组AAV(rAAV)载体都是基于构成该属原型的血清型2(AAV2)。已经采取了许多方法来改善AAV载体的产生,但目前使用最广泛的两种原则不同的策略,具体取决于如何提供腺病毒辅助因子。一种方法依赖于野生型腺病毒感染到稳定携带AAV代表/帽基因的细胞系以及AAV载体DNA中;另一种方法是无辅助方法,基于对宿主细胞(如HEK293细胞)中AAV产生所需的所有元件进行无腺病毒瞬时转染(2)。
它涉及AAV生产细胞与3个质粒的共转染:
(1)携带目的基因的含AAV ITR的质粒;
(2)携带AAV Rep-Cap的质粒;
(3)提供从腺病毒分离的辅助基因的质粒。
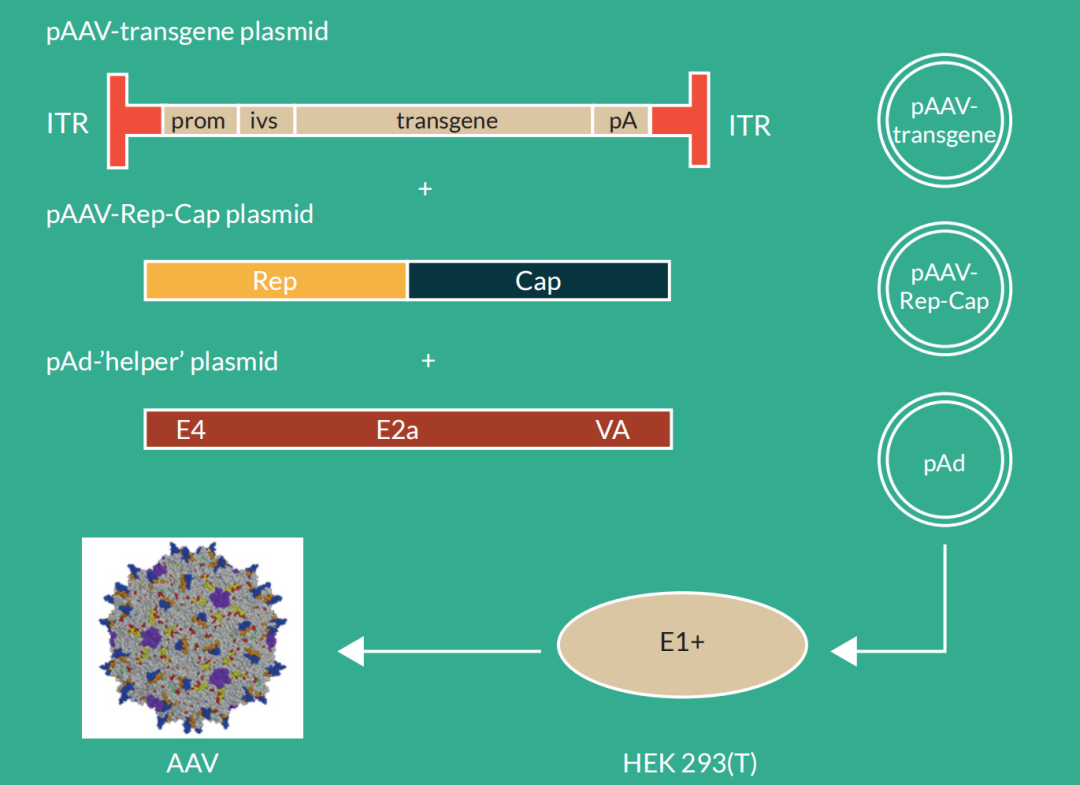
图2.AAV载体组装流程
重组腺相关病毒(rAAV)载体被大量用于体内基因转移,是靶向遗传性疾病、遗传性疾病和许多其他疾病的有前途的治疗方法。动物模型和正在进行的临床试验的结果表明,具有不同血清型的AAV载体对许多不同的组织具有巨大的潜力,包括视网膜,中枢神经系统(CNS),一些内脏或骨骼肌。为了将这些发现转化为临床应用,还需要解决一些问题。
一个主要的挑战是AAV衍生基因疗法的潜在免疫毒性,其形式是针对AAV衣壳抗原的有害免疫反应,这可能会抑制治疗效果。不需要的免疫反应被认为主要受到缺乏目的转基因的空AAV衣壳的影响。因此,准确表征几种感染性定义测量值(如AAV基因组滴度,感染滴度或总AAV衣壳滴度)对于提高和确保AAV衍生基因疗法的有效性和安全性是必不可少的。
腺相关病毒AAV特异性抗体的应用
Acnovia使用不同血清型(AAV2、6、9)的AAV完整病毒颗粒和部分衣壳蛋白(VP1)作为抗原进行免疫反应,通过噬菌体展示等淘选方法获得相应的单克隆抗体序列后进行重组表达,我们获得了有亲和力的重组抗体蛋白,可用于Dotblot半定量检测AAV衣壳滴度。
除了AAV抗体产品,ELISA一直是检测抗体滴度的经典和可靠方法。Acnovia将在AAV特异性抗体的基础上开发配套的腺相关病毒(AAV)ELISA滴度检测试剂盒(3)。该ELISA试剂盒的捕获抗体,可识别野生型、重组型或者组装的空AAV衣壳,而不会识别未组装的AAV蛋白,因此结果准确,可重复性高。尤其适合用于rAAV特征鉴定和制备方法优化。
订购信息: